A Revolução dos Medicamentos Genômicos
O setor farmacêutico foi historicamente limitado na forma como pode abordar doenças. Com o elevado entendimento de doenças e novas tecnologias terapêuticas, a comunidade médica agora tem oportunidades adicionais para tratar e, finalmente, curar doenças.
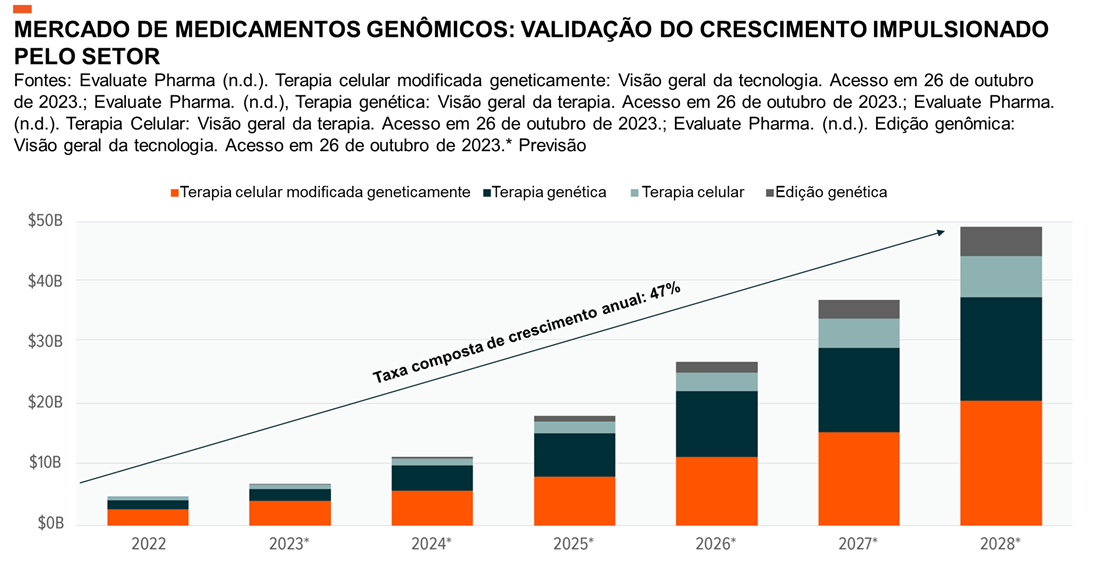
Uma das áreas mais novas de desenvolvimento são os medicamentos genômicos. Desde a primeira aprovação em 2010, existem agora 22 tratamentos aprovados nos Estados Unidos para uma ampla gama de doenças.1 Acreditamos que 2023 marcará o ano de lançamento na área de medicamentos genômicos e o início do mercado de edição genética, que deverá valer quase $50 bilhões até 2028.2
De todas as tecnologias, acreditamos que a indústria de medicamentos genômicos valerá $50 bilhões até 2028, acima dos apenas $5 bilhões em 2022.3,4,5,6
Principais Conclusões
- Medicamentos genômicos oferecem à comunidade médica novas oportunidades de tratamento de doenças. Combinada a um perfil risco-recompensa favorável, esta área tem experimentado investimento elevado que pode acelerar seu crescimento e sua adoção.
- Apesar dos custos iniciais altos, medicamentos genômicos podem ser menos caros do que as terapias tradicionais ao longo prazo, pois tipicamente reduzem a necessidade de tratamentos contínuos, hospitalizações e outas despesas de assistência médica associadas a doenças crônicas ou graves.
- A indústria genômica ainda está na infância, portanto o processo de fabricação é moroso e ineficaz. No entanto, existem técnicas sendo refinadas que podem dramaticamente reduzir os custos iniciais, provavelmente desencadeando adoção mais ampla.
Introdução a Medicamentos Genômicos
Medicamentos genômicos, tais como terapias celular e genética, são uma categoria terapêutica relativamente nova que potencializa informações genéticas de uma pessoa para personalizar a intervenção de acordo com suas necessidades específicas. Existem atualmente quatro tecnologias primárias:
- Edição Genética: Edição de partes do genoma removendo, adicionando ou alterando o DNA.
- Terapia Genética: Substituindo um gene defeituoso ou faltante nas células de um paciente por uma versão saudável daquele gene.
- Terapia Celular: Transplantando células humanas saudáveis para substituição ou reparação de tecido e/ou células danificadas.
- Terapia Celular Modificada Geneticamente: Transferindo células modificadas geneticamente para combater a doença.
Embora os medicamentos genômicos possam contar com algumas tecnologias diferentes, todas elas possuem um estimado perfil de recompensa mais elevado do que a indústria farmacêutica como um todo.

Devido ao perfil de risco-recompensa favorável, não é surpresa que o desenvolvimento de medicamentos genômicos tenha sido priorizado pela indústria farmacêutica. Existem atualmente mais de 1.300 testes clínicos ativos de terapias celular e genética em todo o mundo englobando todas as doenças.7 Espera-se que este nível de pesquisa e desenvolvimento (P&D) acelere aprovações da medicina genômica, continuando a tendência que vimos nos últimos anos.
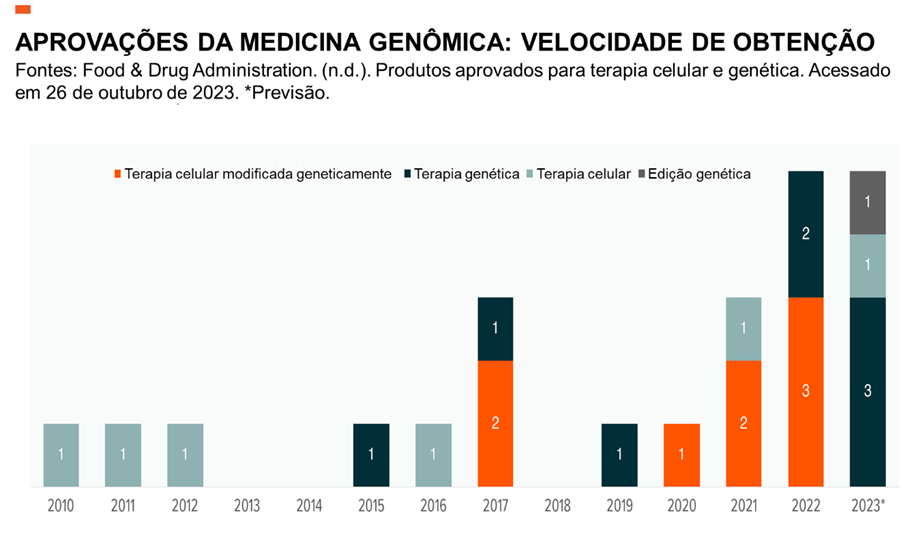
Embora o potencial para adoção geral de medicamentos genômicos seja vasto, identificamos três catalizadores primários para adoção a curto prazo:
- Adoção no tratamento precoce: Medicamentos genômicos são uma categoria relativamente nova e frequentemente chegam com preços mais elevados. Propriamente dito, historicamente temos visto que são um tratamento de último recurso. Esforços recentes, no entanto, apontam para eficácia aprimorada em pacientes pré-tratados, destacando o potencial da categoria e abrindo portas para melhores resultados e rápido crescimento de receita. Para outras informações sobre terapias celulares em pacientes com câncer pré-tratados, consulte ASCO Annual Meeting 2023: Precision Oncology Achieving Widespread Adoption (Encontro Anual ASCO 2023: Oncologia de Precisão Alcançando Adoção Geral).
- Replicando o Sucesso em Novas Categorias de Doença: Até agora, temos visto terapias celular e genética bem-sucedidas e ganhando aprovações em um concentrado conjunto de doenças, notavelmente distúrbios associados ao sangue como anemia falciforme ou linfoma não Hodgkin. Esforços recentes feitos por companhias farmacêuticas e de biotecnologia apontam para sucesso potencial em novas categorias. Notavelmente vimos esforços para terapias CAR-T em distúrbios autoimunes como lúpus e colite ulcerativa e edição genética CRISPR em distúrbios neurológicos como Alzheimer.8,9
- Modalidades Mais Novas Próximas de Receber Aprovação: A tecnologia de edição genética tem sido uma esperança farmacêutica por anos e 2023 pode marcar o ano da primeira aprovação. CRISPR Therapeutics e Vertex Pharmaceuticals estão aguardando aprovação da Agência de Administração de Medicamentos e Alimentos (FDA) de seu tratamento experimental, exa-cel. Este tratamento permite que cientistas editem partes do genoma removendo, adicionando ou alterando seções da sequência do DNA de um paciente. Se aprovado, espera-se que o exa-cel alcance vendas na ordem de $2,6 bilhões até 2028.10 Para outras informações sobre o exa-cel, consulte Another Year of Blockbuster Drug and Treatment Approvals Possible in 2023 (Mais um ano de aprovações de medicamentos e tratamentos de grande sucesso, possíveis em 2023).
Medicamentos Genômicos: Análise de Valor do Preço
Novas categorias terapêuticas oferecem alternativas de tratamento único para doenças complexas e, portanto, vêm com preços por dose mais elevados do que a maioria dos medicamentos. Embora os tratamentos pareçam mais caros no valor nominal, novos métodos oferecem benefício econômico e experiência aprimorada ao paciente.
Estudo de Caso: Hemofilia A
Hemofilia A é um distúrbio genético causado por Factor VIII, proteína importante para coagulação, faltante ou defeituoso. Este distúrbio pode resultar em sangramento espontâneo ou sangramento desproporcional seguido de ferimento.
Roctavian é uma terapia genética única que reduz as taxas de sangramento em 85%.11 Embora o custo por dose seja significativamente mais alto, $2,5 milhões nos EUA e €1,5 na Europa, a infrequência de administração versos tratamentos alternativos concede ao Roctavian economias significativas no custo com cuidados de saúde de até US$ 7,9 milhões.12 Tratamentos alternativos ao Roctavian incluem:
- Hemlibra é uma injeção administrada uma vez por semana que pode resultar em custos anuais de $482.000.13
- Factor VIII, é administrada via infusão, tão frequentemente quanto todos os dias. Isto resulta em custos anuais estimados em $265.000.14
Espera-se que o Roctavian alcance vendas até 2028 na ordem de $1,4 bilhão, tornando-o o terceiro tratamento com maior renda para Hemofilia A.15

Apesar dos custos iniciais mais elevados, as terapias celular e genética oferecem economias substanciais no longo prazo reduzindo a necessidade de tratamentos contínuos, hospitalizações e outras despesas de assistência médica com doenças crônicas ou graves. Dado o propósito curativo das terapias genéticas, é necessária uma estrutura diferente de precificação. Por exemplo, algumas empresas criaram políticas baseadas em resultado. A Bluebird bio oferecerá até 80% de reembolso do preço de sua terapia genética para talassemia, Zynteglo, se o paciente não experimentar resposta constante em até dois anos após sua administração.16
Caminho a Seguir: Reduzir Preços de Fabricação com Expansão da Adoção
Embora os medicamentos genômicos já ofereçam economia de custo a longo prazo, existe um potencial para redução de custos ao longo do tempo através de melhorias nas técnicas de fabricação.
Atualmente, a fabricação de medicamentos genômicos é complexa. Tomam-se duas a três semanas para produção de terapias celulares e até três meses para produção de terapias genéticas, com custos de insumos variando entre $100.000 e $300.000 por dose.17,18,19

Métodos experimentais de fabricação – como fabricação alogênica – procuram melhorar os custos de fabricação, os prazos de entrega e o fornecimento.
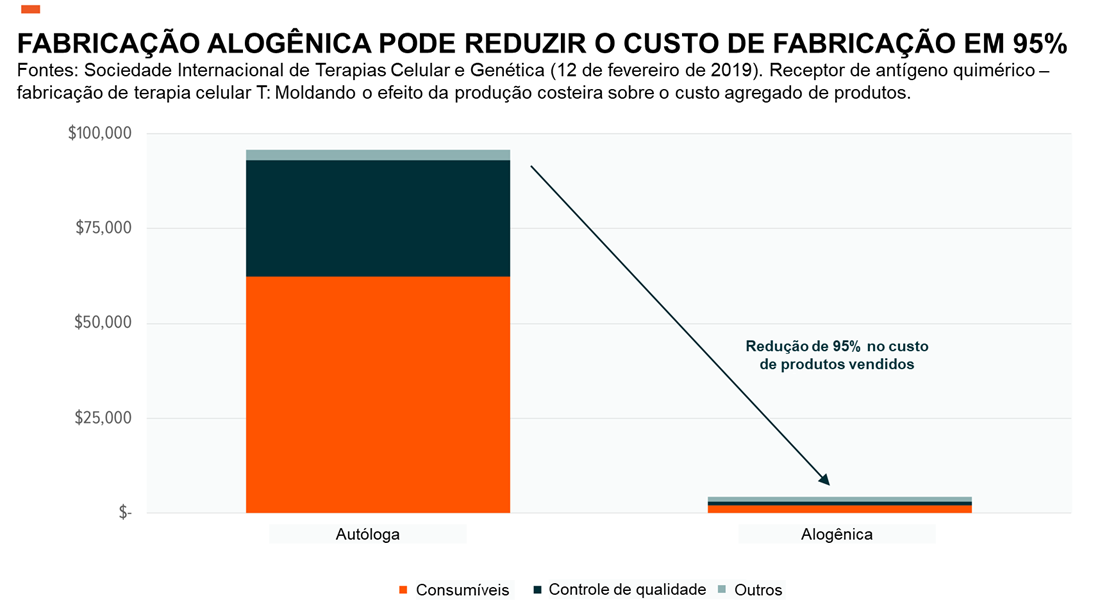
A fabricação atual conta com abordagem autóloga na qual as células T são derivadas do paciente. Por outro lado, um a CAR-T alogênica usa células derivadas de um doador como base para o tratamento. Esta abordagem permitiria um processo de fabricação escalável “pronto para uso”, o que significa que as terapias podem ser fabricadas em grandes lotes de tecidos derivados de um doador em vez de lotes únicos usando tecidos do próprio paciente. Se implantada, a fabricação alogênica pode reduzir o custo de fabricação em 95%.20
Conclusão: A Medicina Genômica Pode Estar Preparada para Crescimento Explosivo
Medicamentos genômicos têm potencial para revolucionar a assistência médica, possivelmente oferecendo a pacientes opções de tratamentos mais efetivos, mais baratos e mais convenientes do que as terapias atuais. Preços iniciais mais elevados dos medicamentos genômicos têm sido um impedimento para adoção mais ampla, porém, os custos a longo prazo já são menos caros para alguns tratamentos relacionados às terapias tradicionais e prevemos os custos iniciais caindo dramaticamente conforme os processos contínuos de fabricação melhoram ao longo do tempo. Com potencial tão vasto, muitas companhias podem se beneficiar do crescimento de medicamentos genômicos. Companhias de biotecnologia seriam os prováveis beneficiários primários, porém, as grandes companhias farmacêuticas e as envolvidas em especialidades médicas e serviços de cuidados médicos podem igualmente se beneficiar. Um ETF tal como ETF Global X Genômica & Biotecnologia oferece vasta exposição a este tema existente.


